Basi epidemiologiche
Per conoscere le modalità di diffusione e il grado di severità degli agenti patogeni a potenziale pandemico è fondamentale pianificare strategicamente l’individuazione precoce, la valutazione del rischio e il controllo delle infezioni.
Agenti patogeni
Gli agenti patogeni a potenziale pandemico sono virus, batteri e altri microrganismi in grado di diffondersi rapidamente a livello mondiale nella parte di popolazione non protetta. Le caratteristiche tipiche di questi agenti patogeni, nuovi o mutati che siano, sono l’elevata trasmissibilità, la scarsa o assente immunità nella popolazione e il loro potenziale di virulenza e letalità. Gli agenti patogeni pandemici sono spesso di origine zoonotica: gli animali possono fungere da serbatoi e trasmetterli all’uomo.
Nel 2024 l’Organizzazione mondiale della sanità (OMS) ha pubblicato i risultati di una valutazione di 1652 agenti patogeni in termini di potenziale pandemico basandosi sulla loro trasmissibilità e virulenza nonché sulla disponibilità di contromisure mediche. Tra questi sono stati definiti prioritari 34 patogeni oggetto di una ricerca avanzata e potenzialmente in grado di scatenare un’emergenza sanitaria di portata internazionale o una pandemia. In questa categoria si collocano soprattutto patogeni respiratori virali, in particolare i virus dell’influenza e i coronavirus, che hanno già causato diverse pandemie dall’inizio del 20 secolo (tabella 1). Alla luce di queste esperienze, il Piano pandemico svizzero si concentra sui virus respiratori e considera un ampio ventaglio di scenari possibili. È necessario creare le basi per una preparazione e una risposta adeguate a una pandemia tenendo in debita considerazione le sfide causate da agenti patogeni nuovi e mutati.
Virus influenzali
L’influenza è una malattia infettiva acuta provocata da virus influenzali della famiglia Orthomyxoviridae, che sono suddivisi nei tipi A, B, C e D in base alle loro proprietà antigeniche. I tipi A e B hanno la maggiore rilevanza epidemiologica nell’essere umano. Sono virus a RNA avvolti con otto segmenti di genoma. Possiedono due proteine di superficie, l’emoagglutinina (H) e la neuraminidasi (N), che svolgono un ruolo importante nella replicazione e nella diffusione del virus nell’organismo ospite. Nei virus influenzali di tipo A si conoscono 18 varianti di emoagglutinina, denominate da H1 a H18, e 11 varianti di neuraminidasi, denominate da N1 a N11.
Coronavirus
I coronavirus (famiglia Coronaviridae) sono un gruppo di virus a RNA che possono provocare diverse malattie negli esseri umani, ma anche negli animali. Devono il loro nome alla proteina spike che forma delle protuberanze sulla superficie del virus facendolo sembrare una corona. La spike funge da legante per aderire a recettori specifici sulla superficie cellulare.
Esistono quattro coronavirus umani (HCoV-229E, HCoV-NL63, HCoV-OC43, HCoV-HKU1), che causano prevalentemente lievi sintomi da raffreddamento. Nonostante la loro diffusione in tutto il mondo, le infezioni hanno un decorso lieve o asintomatico nella maggior parte delle persone. I decorsi gravi e le complicazioni sono rari e riguardano soprattutto le persone immunodepresse o anziane. Dall’inizio del 20° secolo hanno acquisito particolare rilevanza tre nuovi coronavirus zoonotici che hanno causato focolai infettivi, epidemie e pandemie.
Numerosi coronavirus circolano nelle popolazioni animali, in particolare nei pipistrelli, nei roditori e in alcune specie di animali da reddito. Le mutazioni genetiche nei virus possono portare a una diversa trasmissibilità all’uomo e indurre infezioni. Nel caso del SARS-CoV, la civetta delle palme mascherata (una specie del genere Paguma) è stata identificata come possibile ospite intermedio, mentre i dromedari svolgono un ruolo importante per il MERS-CoV. Anche nel caso del SARS-CoV-2 molti specialisti ipotizzano che abbia avuto origine dai pipistrelli e sia passato all’uomo da un ospite intermedio sconosciuto. Il rischio che altri coronavirus zoonotici si trasmettano all’uomo permane e sottolinea l’importanza dell’approccio One Health.
Evoluzione
L’evoluzione dei virus respiratori è guidata da diversi meccanismi che accrescono la loro varietà genetica, quindi possono influenzarne le caratteristiche. Due fenomeni svolgono un ruolo decisivo nella nascita di nuovi virus influenzali:
- la deriva antigenica (antigenic drift) si basa su piccoli cambiamenti (mutazioni puntiformi) nei geni delle proteine di superficie emoagglutinina (H) e neuraminidasi (N), che modificano le proprietà antigeniche del virus e danno origine a nuove varianti. La continua deriva antigenica è responsabile delle ondate stagionali di influenza, dato che la popolazione è solo parzialmente immune al virus mutato. Ne consegue che i vaccini antinfluenzali devono essere adattati ogni anno ai ceppi virali in circolazione;
- lo spostamento antigenico (antigenic shift) deriva dallo scambio di segmenti genici tra due diversi sottotipi e porta a un cambiamento più esteso nel genoma dei virus influenzali rispetto alla deriva antigenica. Lo spostamento antigenico può dare origine a un sottotipo completamente nuovo che può coinvolgere l’emoagglutinina e la neuraminidasi singolarmente o contemporaneamente. Sino ad oggi lo spostamento antigenico è stato constatato solo nei virus dell’influenza A. Questo processo è strettamente correlato all’insorgenza di pandemie, poiché il nuovo virus non è riconosciuto dalle difese immunitarie della popolazione, con il rischio che si diffonda rapidamente e su vasta scala.
Anche nei coronavirus le mutazioni puntuali nel gene della proteina di superficie (spike) possono portare a una graduale diminuzione della risposta degli anticorpi, analogamente a quanto avviene con la deriva antigenica dei virus influenzali. Inoltre, la ricombinazione dei virus nel caso di una co-infezione con diversi coronavirus porta allo scambio di segmenti genomici che possono originare varianti diverse in termini di trasmissibilità e virulenza.
Vie di trasmissione
La via di trasmissione di un agente patogeno è un fattore decisivo per la dinamica e il controllo della sua diffusione. I patogeni utilizzano diversi meccanismi per passare da un organismo ospite al prossimo. La tabella 2 riporta alcuni esempi delle vie di trasmissione di alcuni agenti patogeni con e senza potenziale pandemico. Per elaborare misure di prevenzione e di controllo efficaci è necessario comprendere a fondo questi meccanismi. Generalmente, la via di trasmissione principale di un agente patogeno è determinata sulla base di dati epidemiologici. La maggior parte dei patogeni può diffondersi attraverso diverse vie; tuttavia, le misure di prevenzione e di controllo si concentrano spesso sulla principale.
Le vie di trasmissione dei virus respiratori meritano una particolare attenzione in considerazione del potenziale pandemico e alla luce delle esperienze passate. Le principali vie di trasmissione sono la trasmissione aerogena (goccioline e aerosol), il contatto diretto con le mani e il contatto indiretto tramite superfici contaminate. In passato la trasmissione aerogena era stata suddivisa in due gruppi: la trasmissione per goccioline, riferita all’infezione causata da particelle di dimensioni maggiori che sedimentano rapidamente e la cui propagazione non supera il raggio di 1–2 metri dalla fonte infetta, e la trasmissione per aerosol riferita all’infezione causata da particelle più piccole, con tempi di sospensione più lunghi, che possono coprire anche distanze maggiori soprattutto all’interno di un ambiente chiuso. Anche sulla scorta delle esperienze fatte con la COVID-19, questa dicotomia si è rivelata troppo semplicistica, oltre che errata in base alle leggi fisiche. La «trasmissione per goccioline» è spesso causata da goccioline liberate nell’aria (p. es. mentre si parla o si starnutisce) e la «trasmissione per aerosol» può avvenire in particolare nelle vicinanze di una persona infetta. In caso di una cattiva aerazione dei locali è possibile anche una trasmissione a distanza. In proposito l’OMS utilizza provvisoriamente i termini inglesi «spray» e «inhalation».
Morbilità e mortalità
La morbilità indica la frequenza o la portata di una malattia infettiva in una popolazione o in un determinato gruppo della popolazione. La mortalità, invece, rivela la frequenza dei decessi causati dall’agente patogeno in una popolazione o in un determinato gruppo della popolazione. Gli agenti patogeni pandemici o potenzialmente pandemici possono variare notevolmente in termini di morbilità e mortalità. Se alcuni patogeni inducono prevalentemente sintomi lievi e solo una parte molto esigua della popolazione si ammala gravemente, con altri il rischio di decorsi gravi e di esiti fatali è elevato, soprattutto per persone con patologie preesistenti o un sistema immunitario debole. Il rischio di ammalarsi e di morte è determinato anche da fattori quali l’età, la gravidanza e le condizioni socioeconomiche.
Le ripercussioni sulla salute pubblica non risultano solo dalla cifra assoluta degli ammalati e dei decessi, ma anche dalla dinamica della diffusione. Gli agenti patogeni pandemici possono portare rapidamente le strutture sanitarie ai limiti delle loro capacità, soprattutto se le unità di terapia intensiva hanno risorse limitate. Per la pianificazione strategica della preparazione e della risposta a una pandemia è dunque indispensabile considerare sia le caratteristiche epidemiologiche di questi patogeni sia le caratteristiche cliniche della malattia che causano. Questi dati consentono di valutare il rischio in modo continuativo e di estrapolare scenari sul carico del sistema sanitario.
Un importante indicatore della morbilità è il tasso d’attacco che esprime la quota di infetti da un agente patogeno in una popolazione o in un determinato gruppo della popolazione. La suddivisione in casi asintomatici, sintomatici e diagnosticati consente di trarre conclusioni sulle catene di infezione non riconosciute e la sorveglianza tramite il sistema di dichiarazione. Per valutare il grado di severità clinica della malattia vengono utilizzati diversi altri indicatori. Il tasso di ospedalizzazione misura la quota di persone infette che devono essere ricoverate in ospedale a causa della loro patologia. Il tasso di terapia intensiva descrive le persone che richiedono cure in unità di medicina intensiva. In questa categoria rientrano anche le conseguenze a lungo termine di un’infezione, per esempio l’encefalomielite mialgica/sindrome da stanchezza cronica (ME/CFS).
I principali indicatori della mortalità sono il tasso di letalità apparente e il tasso di letalità effettivo. Il primo si riferisce alla percentuale di casi diagnosticati di persone che muoiono a causa della malattia, mentre il secondo include tutte le persone infette, cioè anche le infezioni non rilevate. Infine la sovramortalità indica il numero di decessi superiori alle attese causati da un agente patogeno.
Dinamica di diffusione
Gli agenti patogeni possono diffondersi in una popolazione secondo diverse modalità. Si parla di focolaio quando si registra un aumento improvviso di casi di infezione in un’area e in un periodo di tempo chiaramente delimitati. L’epidemia indica invece una situazione in cui l’agente patogeno continua a propagarsi (aumento dell’incidenza) in una regione o in una popolazione più ampia per un periodo di tempo prolungato. A differenza dell’epidemia, l’endemia è contrassegnata dall’incidenza stabile di un agente patogeno senza che si registri un numero insolitamente elevato di casi di malattia. Se un’epidemia si manifesta in più continenti e coinvolge gran parte della popolazione mondiale si parla di pandemia.
La trasmissione di agenti patogeni può provocare una crescita esponenziale di casi di infezione, in particolare se molte persone sono suscettibili al contagio e il controllo delle infezioni è assente o insufficiente. Ne sono un esempio caratteristico le ondate epidemiche, nelle quali l’incidenza inizialmente sale, raggiunge un picco, quindi torna a diminuire. Nel caso dei patogeni respiratori virali si assiste spesso a un andamento stagionale dettato dalle caratteristiche della trasmissione, che porta a un incremento del numero di malati nei mesi invernali. Inoltre possono succedersi più ondate di infezione, in particolare se l’immunità della popolazione è insufficiente o se insorgono nuove varianti di virus.
Due concetti epidemiologici fondamentali sono decisivi per comprendere questa dinamica di diffusione: il numero di riproduzione e il fenomeno della superdiffusione (superspreading).
Numero di riproduzione
Il numero di riproduzione di base (R0) indica quante persone contagia in media una persona infetta in mancanza di immunità nella popolazione e di provvedimenti volti a contenere l’infezione. Questo indicatore misura quindi il potenziale massimo di diffusione di un agente patogeno in una popolazione completamente suscettibile al contagio. Diversi fattori influenzano R0, tra cui la contagiosità (trasmissibilità) del patogeno, la durata della contagiosità, il numero di contatti tra persone e la mescolanza della popolazione. Il numero di riproduzione effettivo (Rt o Reff) si riferisce invece a una situazione in cui è già presente un certo livello di immunità e/o vengono attuate misure di controllo. Rt cambia nel tempo e fornisce indicazioni sull’attuale andamento dell’epidemia:
- se Rt > 1, l’agente patogeno può diffondersi nella popolazione e i casi di infezione in un determinato periodo aumentano;
- se Rt = 1, il numero dei casi di infezione rimane costante;
- se Rt < 1, il numero dei nuovi casi di infezione diminuisce.
Quanto più Rt è elevato, tanto più difficile è controllare la diffusione di un agente patogeno. Per ottenere una situazione di contenimento all’esordio di un’epidemia, cioè per portare Rt al di sotto della soglia critica di 1, è necessario prevenire un numero di infezioni espresso dalla formula 1-1/R₀. Nel caso di un patogeno con R₀ = 2,5, come all’inizio della pandemia di COVID-19 nel 2020, ciò corrisponde al 60 per cento dei contagi. Se Rt si riduce grazie a misure di controllo, ma rimane al di sopra di 1, si parla di mitigazione, ossia la diffusione di un’ondata di infezioni rallenta. Si riduce così il numero massimo di persone contemporaneamente infette e bisognose di cure ed è possibile evitare un carico eccessivo o un sovraccarico del sistema sanitario.
In una pandemia R₀ e Rt sono indicatori decisivi per prevedere il potenziale di diffusione, valutare costantemente il rischio e la situazione e definire una strategia appropriata di contenimento o mitigazione (controllo dell’infezione).
Superdiffusione
La superdiffusione è il fenomeno in cui poche persone infette causano un numero particolarmente elevato di casi secondari, mentre la maggioranza delle persone contagia solo pochi o nessuno. Può essere influenzata da fattori biologici del patogeno e dell’organismo ospite così come da un comportamento specifico. Un «evento di superdiffusione» si verifica se una persona infetta contagia più persone di quanto sarebbe ipotizzabile secondo il 99° percentile di una distribuzione di Poisson con il valore atteso R₀. Nel caso di un agente patogeno con R₀ = 2,5 si parla di superdiffusione se vengono contagiate più di altre sette persone.
La distribuzione irregolare dei casi secondari è descritta dal fattore di dispersione k. Un suo valore basso (k < 1) indica una variabilità elevata del numero dei casi secondari, pertanto una minoranza delle persone infette (10–20 %) causa la maggioranza dei contagi (80 %). Tra gli agenti patogeni per i quali si verifica spesso una superdiffusione si annoverano il virus dell’ebola, il SARS-CoV e il MERS-CoV. Questo modello di distribuzione non uniforme ha importanti ripercussioni sulla pianificazione strategica e sull’attuazione di provvedimenti per il controllo dell’infezione: il tracciamento dei contatti (contact tracing) è particolarmente efficace se è mirato a eventi di superdiffusione.
Fasi pandemiche
La suddivisione di una pandemia in diverse fasi è uno strumento importante per la pianificazione strategica e l’attuazione operativa dei provvedimenti. Gli obiettivi della preparazione e della risposta a una pandemia si orientano alle diverse fasi di sviluppo. La descrizione chiara e oggettiva di queste fasi aiuta ad adeguare tempestivamente i provvedimenti alla situazione e facilita il coordinamento tra i servizi responsabili.
Il Piano pandemico nazionale distingue quattro fasi basate sulla situazione epidemiologica in Svizzera in relazione a un nuovo agente patogeno:
La durata delle singole fasi può variare notevolmente: i passaggi, per esempio dalla fase interpandemica a quella pandemica, possono essere molto rapidi. Occorre inoltre osservare che le «fasi pandemiche», le «fasi di allerta pandemica» dell’OMS e il «modello basato su livelli» secondo la LEp hanno un focus diverso: le fasi pandemiche rispecchiano la situazione epidemiologica a livello nazionale, mentre le fasi di allerta pandemica dell’OMS si riferiscono agli sviluppi su scala globale. Il modello basato su livelli considera la portata potenziale della crisi in Svizzera.
Valutazione dei rischi e scenari
La valutazione dei rischi e l’elaborazione di scenari sono indispensabili per prevedere le possibili ripercussioni di un agente patogeno pandemico e sviluppare provvedimenti mirati in preparazione e risposta a una pandemia. La valutazione dei rischi consente un’analisi sistematica delle minacce e serve quindi all’individuazione precoce, mentre gli scenari delineano possibili sviluppi e supportano pianificazioni a lungo termine. Ciò è particolarmente importante per i patogeni respiratori virali come i virus dell’influenza e i coronavirus, che possono diffondersi rapidamente in tutto il mondo e per i quali si dispone di sufficienti valori empirici con diversi gradi di gravità.
La valutazione dei rischi e lo sviluppo di scenari si basano sui seguenti metodi scientifici:
- Operational tool on rapid risk assessment methodology: questo strumento messo a punto dal Centro europeo per la prevenzione e il controllo delle malattie (European Centre for Disease Prevention and Control; ECDC) consente una valutazione del rischio rapida, strutturata e riproducibile per nuovi agenti patogeni. Il rischio è determinato sulla base di sette domande come combinazione della probabilità di comparsa e di diffusione dell’agente patogeno e delle potenziali ripercussioni per la salute pubblica valutate sulla base di una matrice di rischio. Lo strumento è utilizzato in particolare nella fase interpandemica e in quella iniziale di una pandemia.
- Pandemic Severity Assessment Framework (PSAF): questo strumento elaborato dai Centers for Disease Control and Prevention (CDC) negli Stati Uniti serve a valutare la trasmissibilità e il grado di severità clinica di una pandemia per una valutazione complessiva dell’impatto potenziale. La trasmissibilità può essere determinata sulla base dell’indice R0 o del tasso d’attacco atteso, mentre il grado di severità clinica è dato da indicatori tra cui il tasso di ospedalizzazione o il tasso di letalità effettivo. Lo strumento viene utilizzato principalmente nella fase iniziale e in quella pandemica. Può tuttavia essere utile anche nella fase interpandemica per l’elaborazione di scenari.
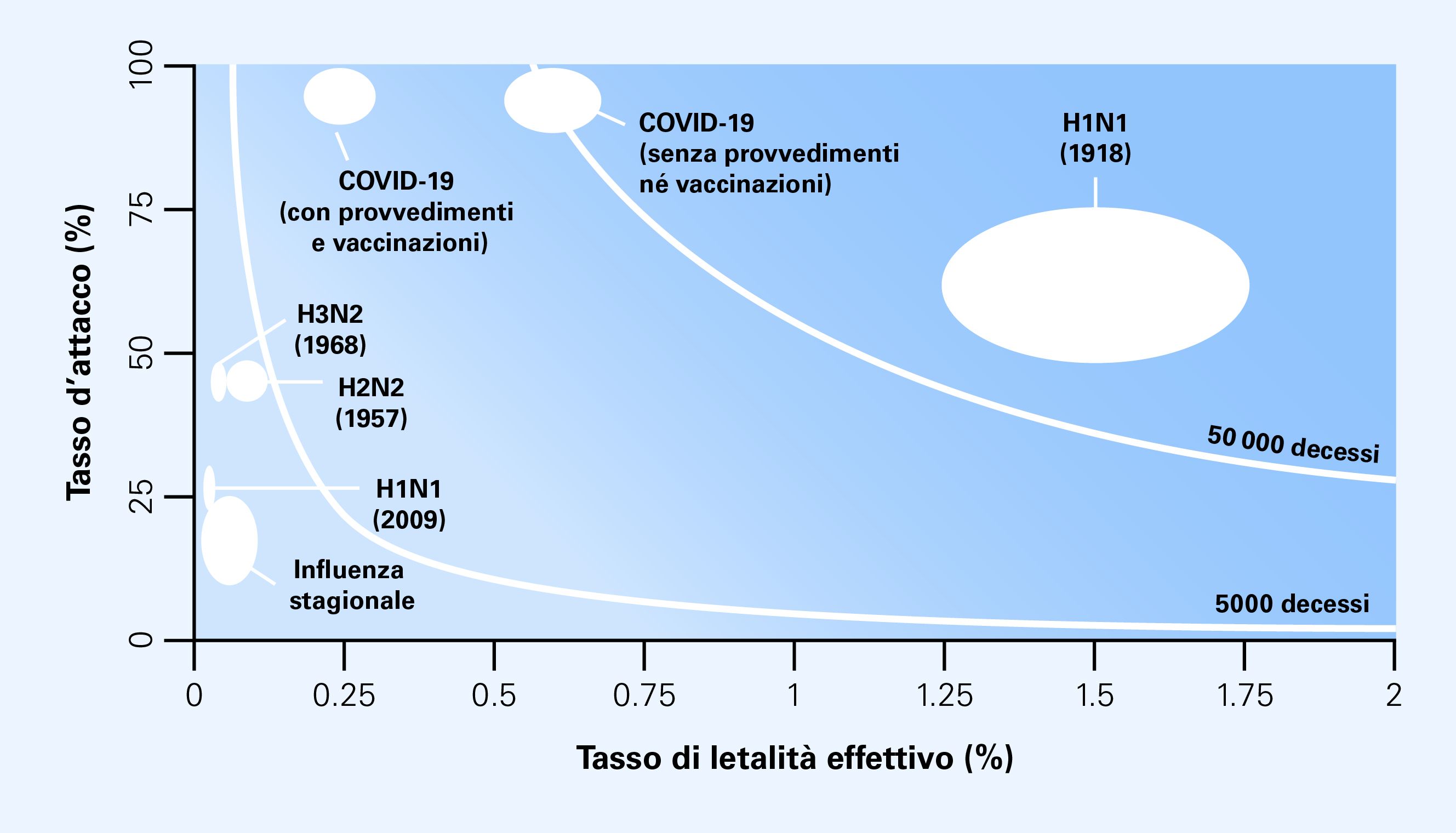
Il grado di severità di una pandemia può essere rappresentato dal numero dei decessi risultanti da un determinato tasso d’attacco e un tasso di letalità effettivo (fig. 1). Ciò consente di confrontare diversi scenari pandemici con le ripercussioni di pandemie passate o dell’influenza stagionale. Questi esempi storici, che spaziano da eventi limitati come l’influenza pandemica H1N1 nel 2009 fino a eventi estremi come la pandemia influenzale del 1918, dimostrano l’enorme variabilità dei possibili scenari. In base alle dimensioni della popolazione svizzera (9 milioni a fine 2024), il grado di severità di una pandemia causata da patogeni respiratori virali può essere approssimativamente suddiviso in tre scenari:
Nella pianificazione strategica devono essere considerati anche l’orizzonte temporale della fase pandemica, il numero di ondate di infezioni e il numero di persone contemporaneamente infette e bisognose di cure. Inoltre, il grado di severità di una pandemia non dovrebbe essere valutato soltanto sulla base del numero atteso di decessi, ma anche con altri parametri, tra cui il numero di malati gravi in diverse fasce di età e gruppi di popolazione o le possibili conseguenze a lungo termine.
Tuttavia, non sempre è possibile valutare il rischio e creare scenari su basi certe, poiché a volte mancano informazioni dettagliate sulla trasmissibilità e sul grado di severità clinica oppure non è possibile determinare questi indicatori con sufficiente precisione. Questi indicatori sono comunque strumenti indispensabili per prevedere possibili sviluppi e approntare provvedimenti opportuni. Il continuo adattamento alle nuove conoscenze scientifiche è quindi fondamentale.

